
Что такое индикатор pH?
Индикатор pH — это общее название органических красителей, которые меняют цвет при изменении pH. Их также называют кислотно-основными индикаторами или нейтрализующими индикаторами. pH, при котором происходит реакция, изменяющая структуру индикатора, отличается в зависимости от индикатора. Поэтому важно выбрать индикатор, который соответствует диапазону pH, который нужно проверить. Фенолфталеин, который меняет цвет в основных растворах, является типичным индикатором pH.
Большинство индикаторов pH часто используются в НИОКР и производстве в обрабатывающей промышленности, а также используются для проверки pH сельскохозяйственных культур и почвы. Кроме того, индикаторы pH уже давно используются в школьном образовании, например, на уроках естествознания, из-за их большого изменения цвета и простоты использования.
Применение индикаторов pH
Поскольку индикаторы pH могут легко определить pH раствора образца, они широко используются, особенно в аналитических приложениях. Например, в обрабатывающей промышленности они часто используются на производственных площадках для проверки точки нейтрализации или для проверки pH сточных вод. В частности, диапазон pH сточных вод, сбрасываемых с заводов в канализацию, устанавливается правительством, поэтому контроль pH сточных вод имеет важное значение.
Кроме того, его иногда используют для проверки pH почвы и продуктов питания в сельском хозяйстве. В частности, измерение pH чрезвычайно важно для стабильного роста урожая, поскольку pH почвы оказывает значительное влияние на то, как растут культуры, а оптимальный pH варьируется в зависимости от культуры и исходного pH почвы в разных регионах.
Принцип индикаторов pH
Цвет индикаторов pH меняется, потому что химическая структура индикаторов pH меняется с изменением pH. Изменение ароматического кольца и положения двойной связи изменяет энергетическое состояние молекулы (энергии HOMO и LUMO), что приводит к изменению длины волны поглощаемого света.
1. Раствор BTB
Рисунок 1. Структурные изменения в BTB
Раствор BTB (бромтимоловый синий) используется в качестве индикаторов pH для различения кислоты и основания, поскольку цвет BTB сильно различается в кислых, нейтральных и основных растворах. Строго говоря, BTB является кислотным, поэтому химическая структура коммерческих продуктов представляет собой натриевую соль.
Когда pH раствора BTB меньше 6,0, почти все BTB образуют соль с натрием, но когда pH больше 7,6, протон гидроксильной группы BTB также десорбируется с образованием двухвалентного аниона. Это структурное изменение приводит к изменению цвета: желтый для pH меньше 6,0, синий для pH больше 7,6 и зеленый для pH между ними, что является суперпозицией цветов двух соединений.
2. Фенолфталеин
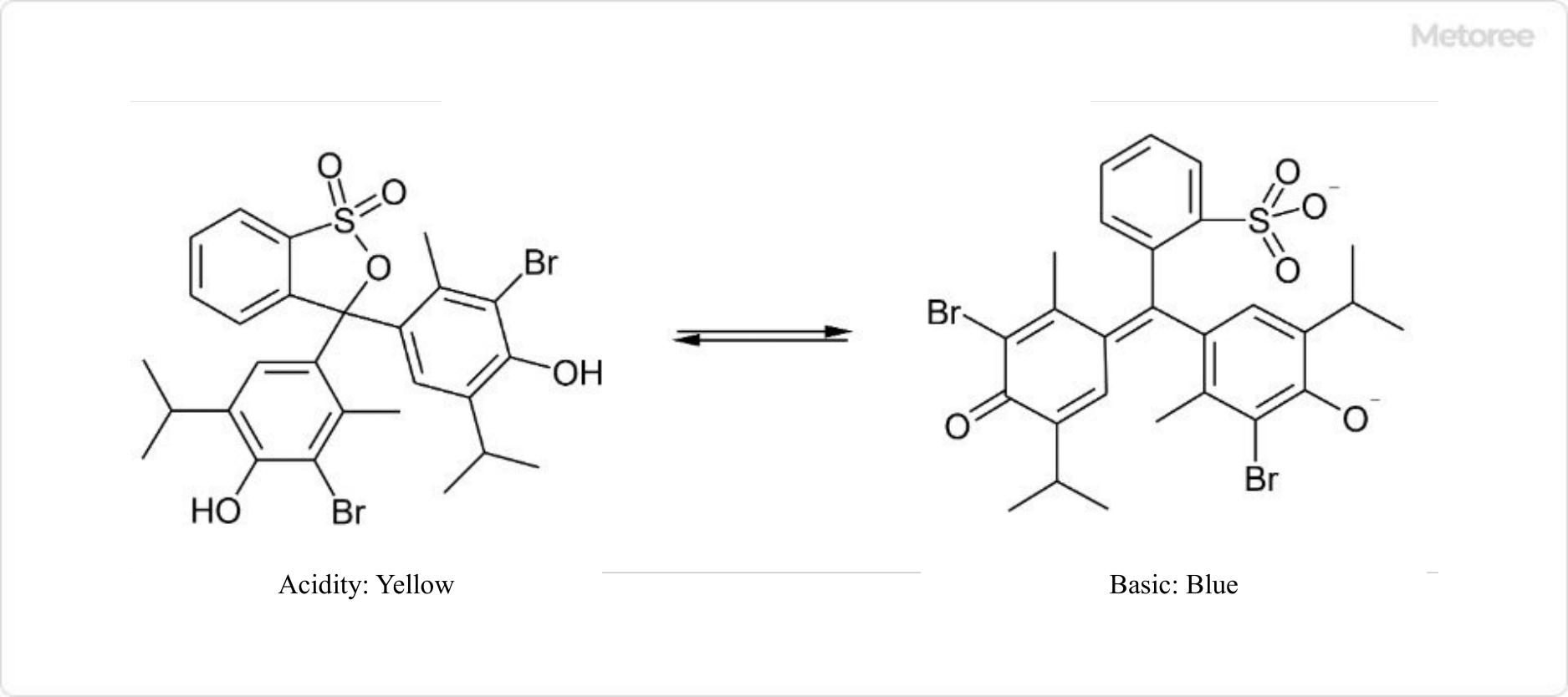
Рисунок 2. Структурные изменения фенолфталеина
Раствор фенолфталеина в индикаторах pH используется для идентификации основных растворов. Его часто используют в школьных научных экспериментах из-за его легко узнаваемой фиолетовой окраски.
Фенолфталеин — это белое твердое вещество, растворимое в этаноле и воде. Растворы фенолфталеина в нейтральных или кислых средах прозрачны, но когда pH превышает 9, эфирная часть расщепляется и превращается в анион, окрашивая раствор в фиолетовый цвет. С другой стороны, при pH выше 10 фенолфталеин претерпевает дальнейшие структурные изменения, а при pH выше 13 фиолетовый раствор снова становится прозрачным и бесцветным.
Другая информация об индикаторах pH
1. Индикаторы pH в обрабатывающей промышленности
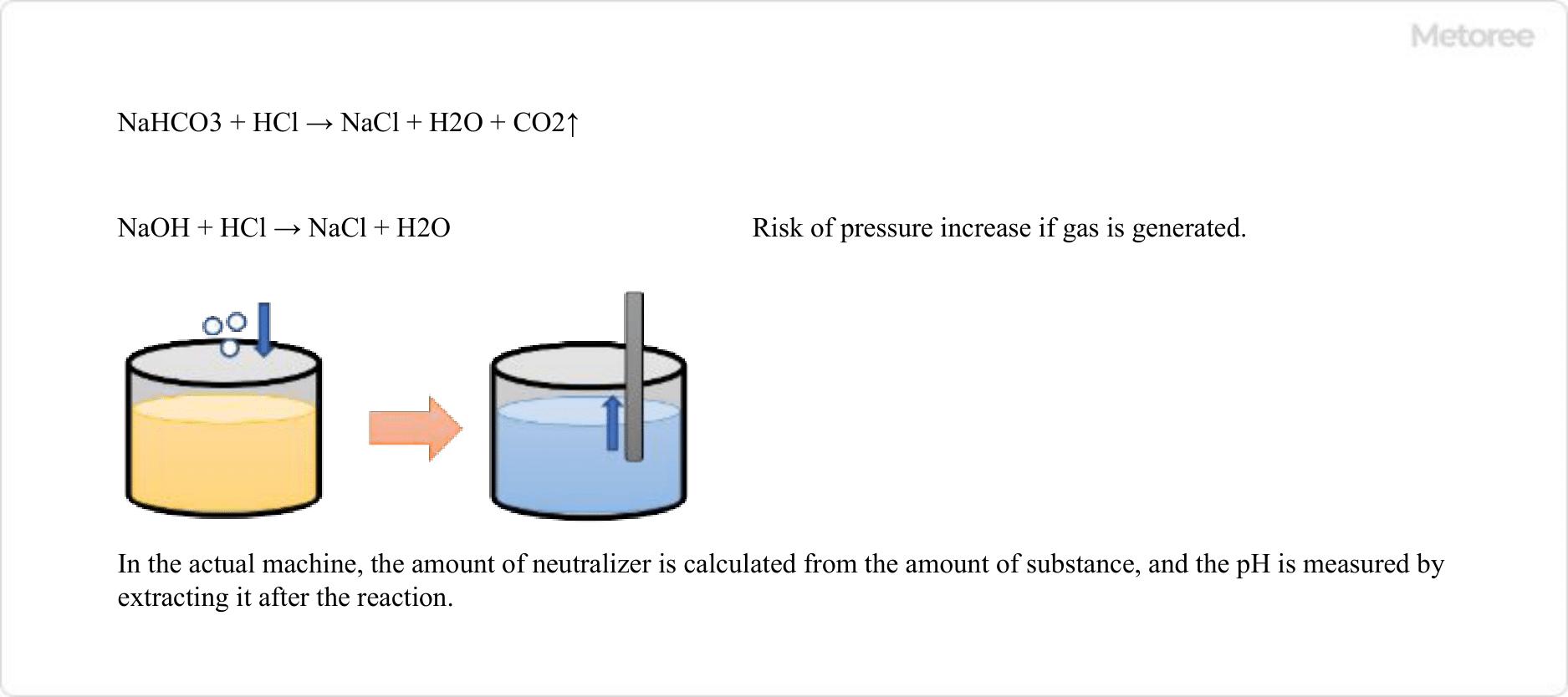
Рисунок 3. Использование индикатора pH в обрабатывающей промышленности
Показатель pH сточных вод, которые предприятия могут сбрасывать в канализацию, устанавливается каждым муниципалитетом и должен быть нейтральным. В случаях, когда объем используемых сточных вод невелик, например, в лабораториях и НИОКР, в качестве нейтрализующего агента используется слабое основание, например, бикарбонат натрия, а индикаторы pH, которые меняют цвет около нейтрального, добавляются в сточные воды для проверки их pH.
Однако нейтрализация с использованием бикарбоната натрия приводит к образованию углекислого газа, который в некоторых случаях не может быть использован на производственных площадках в больших масштабах. В таких случаях нейтрализацию можно проводить с использованием основания или кислоты, такой как соляная кислота или гидроксид натрия, которые не образуют газ.
Поскольку индикатор нельзя добавлять непосредственно в сточные воды на производственной площадке, сточные воды берутся на пробу после очистки и добавляют индикатор для проверки уровня pH.
2. Использование индикаторов pH в сельском хозяйстве
В сельском хозяйстве pH почвы контролируется из-за его значительного влияния на сельскохозяйственные культуры. Кроме того, подтверждение pH часто требуется не только для сельскохозяйственных культур, но и для широкого спектра пищевых продуктов.
Например, для пищевых продуктов, которые растворяются в воде, таких как сухой суп, индикаторы pH могут быть добавлены к пище, растворенной в воде, для простого анализа. Для твердых пищевых продуктов, таких как мясо и рыба, вместо индикаторов pH используется прибор для измерения pH с использованием электрода.
