
Что такое этаноламины?
Этаноламины — это общее название для трех различных соединений: моноэтаноламина, диэтаноламина и триэтаноламина.
Когда мы говорим просто об этаноламинах, мы имеем в виду моноэтаноламин, который является 2-аминоэтанолом. Моноэтаноламин — это жидкость с запахом аммиака, вязкостью и гигроскопичностью. Он также известен как аминоэтиловый спирт или коламин.
Этаноламины классифицируются как опасные вещества 4-го класса. Моноэтаноламин также считается вредным веществом и требует осторожного обращения.
| Химическая формула | C2H7NO |
| Английское название | Этаноламины |
| Псевдоним английского названия | Моноэтаноламин |
| Молекулярный вес | 61.08 |
| Температура плавления | 10 ~ 10,5℃ |
Применение этаноламинов
1. Моноэтаноламин
Моноэтаноламин широко используется в качестве эмульгатора, поскольку он растворим в воде и масле. Он также может использоваться в синтетических моющих средствах, ингибиторах коррозии металлов, косметике, фармацевтических препаратах и сельскохозяйственных химикатах. Кроме того, моноэтаноламин используется для очистки газовых смесей с целью удаления кислых газов.
2. Диэтаноламин
Диэтаноламин может использоваться как эмульгатор в моющих средствах, косметике и восках, а также как смачивающий агент в текстиле.
3. Триэтаноламин
Триэтаноламин используется как основной катализатор в реакциях конденсации, в реакциях органического синтеза, как эмульгатор, пластификатор, антикоррозионная добавка и увлажнитель. Он также используется в анализе как коллектор диоксида азота в атмосфере.
Свойства этаноламинов
Этаноламины обладают свойствами как спиртов, так и аминов. Моноэтаноламин имеет плотность 1,012 г/см3, температуру плавления 10,3°C и температуру кипения 170°C.
Диэтаноламин имеет плотность 1,090 г/см3, температуру плавления 28,0°C и температуру кипения 217°C. Триэтаноламин имеет плотность 1,126 г/см3, температуру плавления 20,5°C и температуру кипения 208°C. Этаноламины хорошо растворяются в воде и ацетоне. Благодаря своей основной природе он поглощает кислотные газы, такие как углекислый газ (CO2) и сероводород (H2S). Он также может реагировать с жирными кислотами, образуя сложные эфиры.
Структура этаноламинов
Рисунок 1. Структура этаноламинов
1. Моноэтаноламин
Моноэтаноламин является как первичным амином, так и первичным спиртом. Его химическая формула C2H7NO, а его молярная масса составляет 61,08 г/моль.
2. Диноэтаноламин
Диэтаноламин имеет вторичный амин и две гидроксильные группы в молекуле. Его химическая формула — C4H11NO2, а его молярная масса — 105,14 г/моль.
3. Триэтаноламин
Триэтаноламин имеет третичный амин и три гидроксильные группы в молекуле. Его химическая формула — C6H15NO3, а его молярная масса — 149,188 г/моль.
Другая информация об этаноламинах
1. Синтез этаноламинов
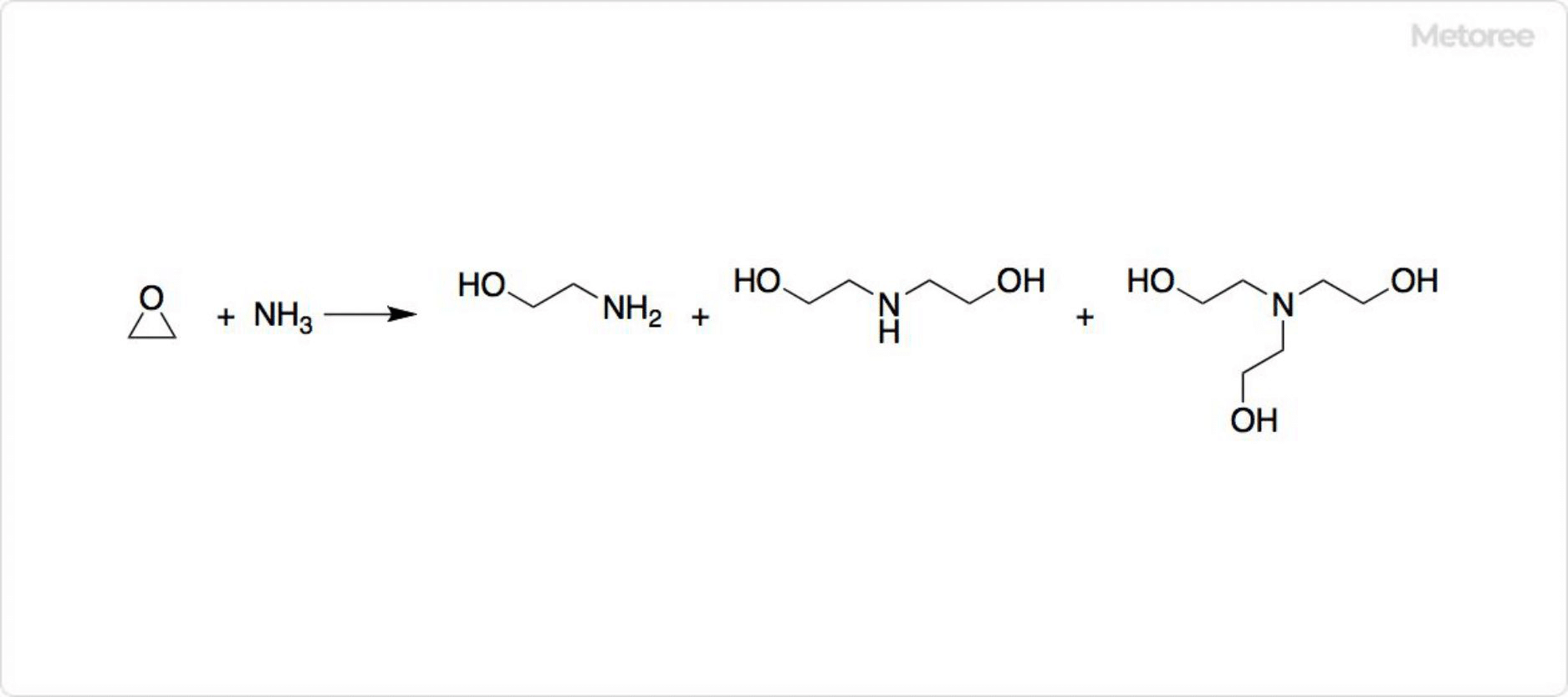
Рисунок 2: Синтез этаноламинов
Моноэтаноламин может быть получен реакцией окиси этилена и аммиака. Однако в зависимости от условий реакции также могут быть получены диэтаноламин и триэтаноламин. Соотношение полученных соединений можно контролировать, изменяя стехиометрическое соотношение исходных материалов.
2. Родственные соединения этаноламинов
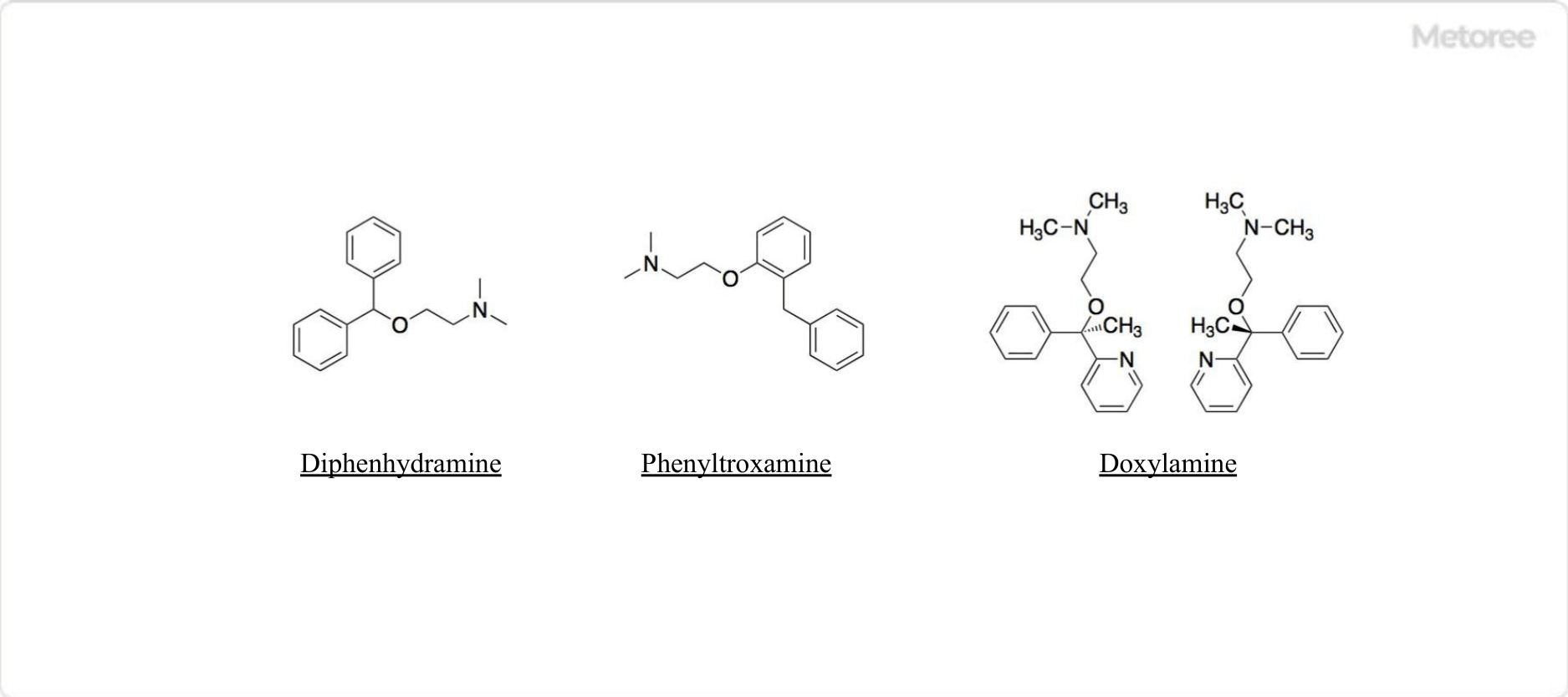
Рисунок 3. Соединения с подструктурой этаноламинов
Этаноламины встречаются в общей структуре антигистаминных препаратов. В частности, в антигистаминных препаратах первого поколения дифенгидрамине, фенилтолоксамине (Percogesic) и доксиламине (Unisom) этиламин связан с дифенилметаном. Это также субструктура этиламина, связанная с дифенилметаном в percogesic и доксиламине (Unisom).
Он по-прежнему считается эффективным веществом при аллергических заболеваниях. Этаноламины в изобилии присутствуют в фосфолипидах и также встречаются в биологических мембранах.
