Все про видеонаблюдение
Все про умный дом
Все о пожарной безопасности
Сейчас читают
 Как ускорить и смотреть ютуб без тормозов и замедленияЕсли Вы на этой странице, то Вам, скорее всего, […]
Как ускорить и смотреть ютуб без тормозов и замедленияЕсли Вы на этой странице, то Вам, скорее всего, […] 10 лучших прогрессивных языков программирования для разработки мобильных приложенийЗнаете ли вы, что мобильные приложения — это не только […]
10 лучших прогрессивных языков программирования для разработки мобильных приложенийЗнаете ли вы, что мобильные приложения — это не только […] 6 важных особенностей, которые следует учитывать при строительстве нового домаСтроительство нового дома – это уникальная возможность […]
6 важных особенностей, которые следует учитывать при строительстве нового домаСтроительство нового дома – это уникальная возможность […]
Гороскоп на Сегодня

Что такое аллен?
Рисунок 1. Основная информация об аллене
Аллен — это органическое соединение со структурой, состоящей из трех атомов углерода, соединенных в линейную цепь двумя двойными связями.
Эти соединения в совокупности называются алленами. Соединение с наиболее простой структурой среди алленов — пропадиен. Пропадиен иногда называют алленом.
Пропадиен может быть синтезирован путем воздействия цинкового порошка на этанольный раствор 2,3-дибромпропена или 2,3-дихлорпропена. С другой стороны, когда пропадиен поглощает серную кислоту и перегоняется с водой, он становится ацетоном.
Применение аллена
Пропадиен, «аллен» в узком смысле, используется как компонент МАПП-газа МАПП-газ представляет собой смесь пропадиена и метилацетилена МАПП-газ используется для пайки и сварки. Он безопасен и прост в транспортировке, но не экономически эффективен.
Соединения, классифицируемые как «аллен» в широком смысле этого слова, не используются в промышленности. Однако аллен очень реактивен и может подвергаться различным реакциям присоединения, что делает его перспективным кандидатом для использования в полезных химических реакциях. Аллен характеризуется своей аксиальной хиральностью.
Свойства аллена
Химические свойства алленов значительно отличаются от свойств обычных алкенов. Аллен очень нестабилен по сравнению с сопряженными и изолированными диенами. Связи C-H в аллене слабее и более кислые, чем связи C-H в винильных группах.
Аллен вступает в реакции циклоприсоединения [2+2] и [4+2]. Формальные реакции циклоприсоединения протекают при использовании катализаторов на основе переходных металлов.
Пропадиен, самая базовая структура аллена, представляет собой бесцветный газ со сладким запахом. Он имеет температуру плавления -136,3°C и температуру кипения -34,4°C. Он практически нерастворим в воде. Он легко разлагается, но очень стабилен и используется в качестве сварочного топлива вместе с метилацетиленом.
Структура аллена
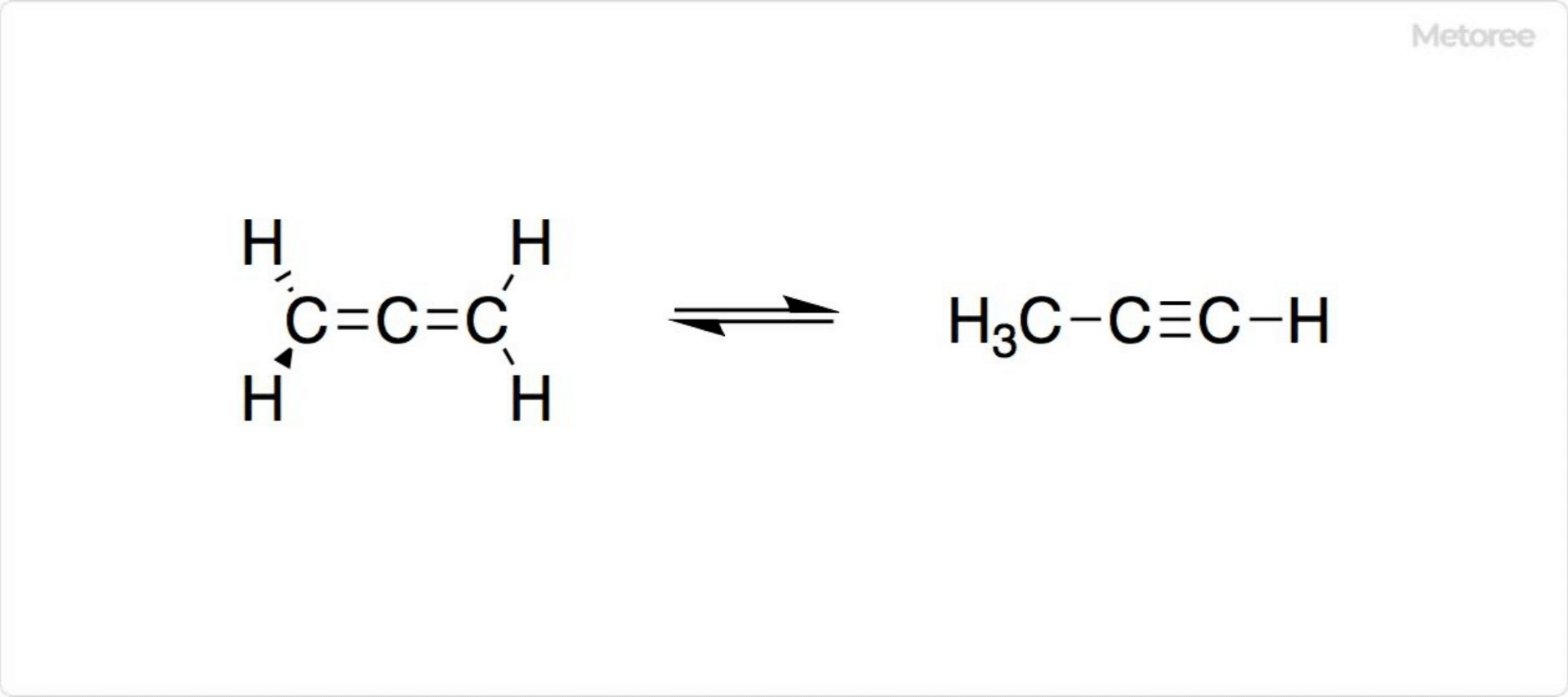
Рисунок 2. Синтез аллена
Структура с двумя или более последовательными двойными связями, как в аллене, называется интегрированной двойной связью. Химическая формула R2C=C=CR2. Название соединения с тремя или более двойными связями подряд — кумулен. Заместители, такие как R2C=C=CR–, где R — алкильная группа аллена, называются алленильными группами.
Самая основная структура аллена, пропадиена, имеет химическую формулу H2C=C=CH2. Пропадиен существует в равновесии с метилацетиленом, который имеет химическую формулу H3C-C3≡CH. Для синтеза аллена часто требуются специальные синтетические методы. Однако в промышленности пропадиен синтезируется из смеси с метилацетиленом.
Другая информация об аллене
1. Геометрическая структура аллена
Центральный атом углерода аллена имеет две сигма- и две пи-связи. Два концевых атома углерода имеют гибридные sp2-орбитали. Три атома углерода образуют линейную структуру с углом связи 180°. Два концевых атома углерода образуют плоскую структуру, и каждая плоскость скручена на 90° в конфигурации.
2. Молекулярная симметрия аллена
Молекулу аллена часто сравнивают с двухлопастным пропеллером. То есть аллен имеет четыре заместителя, и из двух различных концевых плоскостей CH2 через центральный атом углерода идут две оси симметрии вращения 2-го порядка C2, наклоненные под углом 45°.
Существует третья двойная ось вращательной симметрии вдоль оси связи C=C=C, и обе плоскости CH2 являются плоскостями зеркальной симметрии. Исходя из вышеизложенного, симметрия молекулы аллена принадлежит точечной группе D2d, а аллен без заместителей является неполярной молекулой без полного дипольного момента.
3. Изомеры аллена
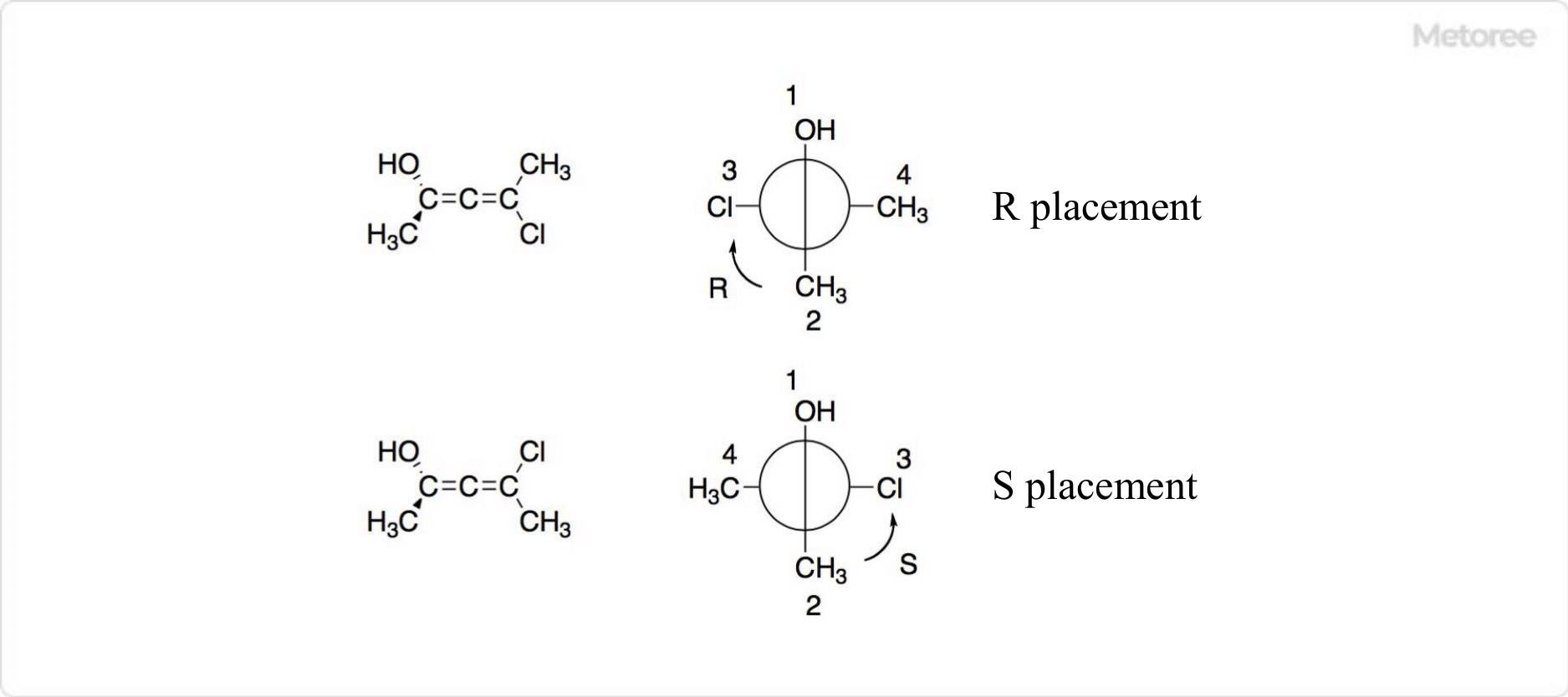
Рисунок 3. Изомеры аллена
Производные, в которых два атома углерода молекулы аллена связаны с двумя разными заместителями, имеют зеркальные изомеры. Конфигурации R и S можно определить по приоритету заместителей, когда молекула аллена рассматривается вдоль ее оси. Передняя сторона предпочтительнее задней, что определяется относительным расположением передней и задней сторон.
Таким образом, аллен обладает необычными оптическими свойствами и используется в качестве строительного блока в синтезе органических материалов.






